シリカは、表面や細孔を利用して物質を吸着します。この吸着機能を利用して水をはじめとして、有害ガスや重金属などの有害物を吸着、最近では二酸化炭素の吸着担体としても注目されています。
このように、よく“吸着”、“吸着”とわれわれの身近でも使用されていますが、いったい吸着ってどんな現象かいまひとつよくわからない??? 。
そういう方もいらっしゃるかと思いますので、今回はシリカの中で重要な機能の一つである“吸着”という機能に注目して解説していきます。
物質の三態
本題の吸着に入る前に、物質の三態についてお話をさせていただきます。
物体は、温度や圧力によってその形が変わります。例えば水は、0℃以下になると固体の氷です。100℃以上になるとすべて気体の水蒸気に形を変えます。0℃から100℃の間では液体の水ではありますが、温度によって少しずつ蒸発して水蒸気になっていきます。このようにあらゆる物質は温度や圧力に応じて、固体・液体・気体という、いずれかの状態をとります。このような三つの状態を『物質の三態』といいます。
物質の状態は、分子の動きやすさの状態を表してます。
気体は分子が自由に空気中を動き回れる状態、固体は分子が押し固められて動けない状態、そして液体はその中間、少しだけ動ける状態です(Fig1)。
ほとんどの物質が固体、液体、気体の順に体積が大きくなるのはそのためです。
しかし例外もあり、水が固体になると液体よりも体積が増えるのは、水素同士の分子間力によります。
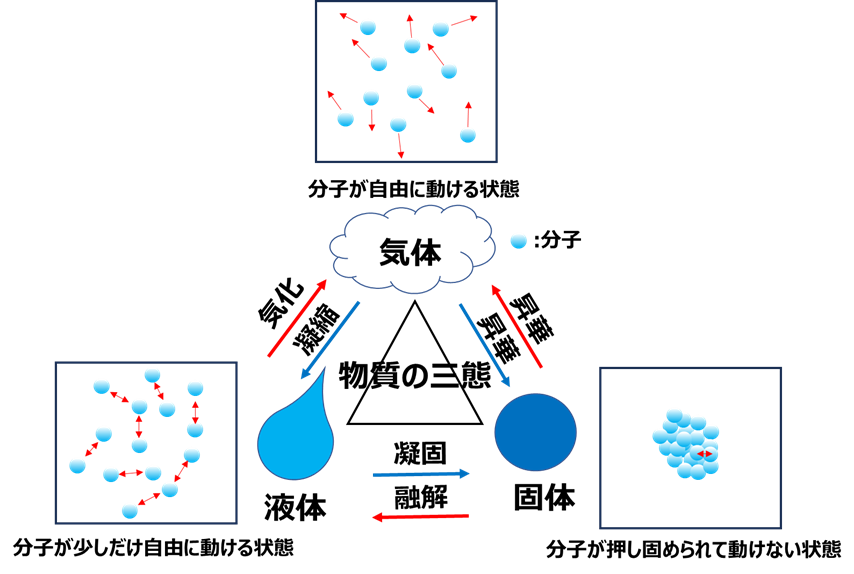
Fig1. 物質の三態と分子の状態1)
このように自由に物体が動き回れるかという状態がキーポイントで、圧力が高まれば、それだけ分子は自由に動き回りにくくなるため凝固しやすくなります。逆に圧力が下がると、分子は自由に動き回りやすくなるので、気化しやすくなります。
Fig2に物質の三態と圧力・気体の相関関係を示します。
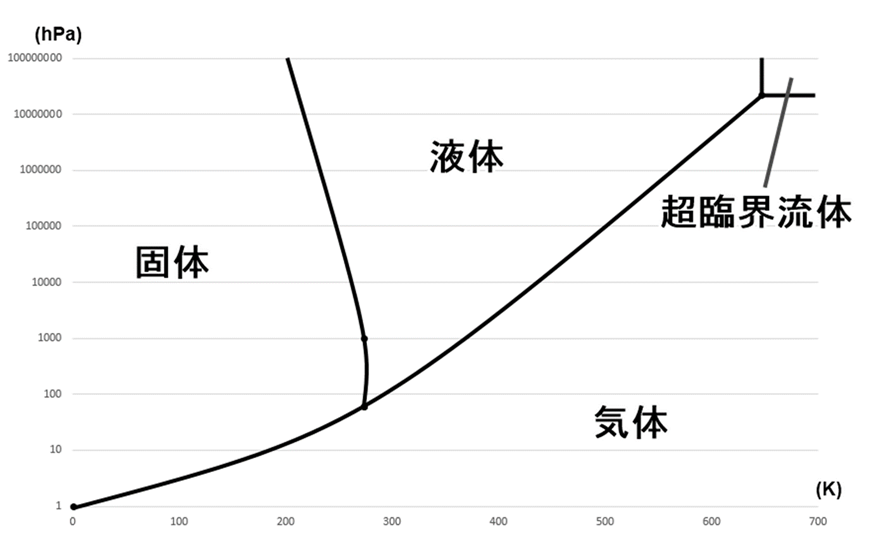
Fig2.物質の三態と圧力・気体の相関関係2)
グラフの縦軸1,000hPaで見ると、横軸の約273K(=0℃)が固体と液体の境目であり、約373K(=100℃)が液体と気体の境目であることが分かります。
このように状態図は、特定の圧力条件下における特定の温度の場合、どのような態を取るかが分かる図となっています。
このグラフの傾きなどは物質によって異なります。また、圧力と温度を高めていくと、ある一定のラインより先は超臨界流体と呼ばれる、液体・気体の区別ができない物質に変化します。
更に、極度の高温条件にした場合、気体からさらにプラズマに変化します。
プラズマは、気体となった分子の運動が熱エネルギーによってさらに高まり、原子が電子と陽子・中性子に分裂(電離)することで生じます。
吸着とは
英語ではadsorptionといい、一般的には吸いつくことです。
化学的には固体に気体が接する時、気体の一部が固体の表面に引きつけられる現象で、固体と液体、液体と液体、液体と気体との場合も起こります。
吸着には大きく分けると、固相吸着と液相吸着の2種類あります。
固相吸着
固相に気相、液相、固相が吸着する現象です。
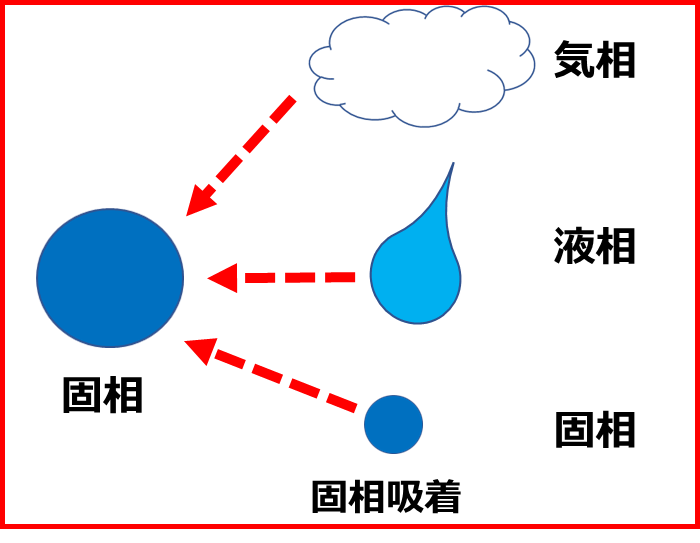
Fig3.固相吸着のイメージ
液相吸着
液相に気相や液相が吸着する現象です。吸着は分子の運動が小さいものが大きいものを引き付けます。固相より液相のほうが分子運動はさかんなため、液相に固相が吸着されることが無く、この場合も固相吸着となります。また、同様に気相や液相にも言えます。
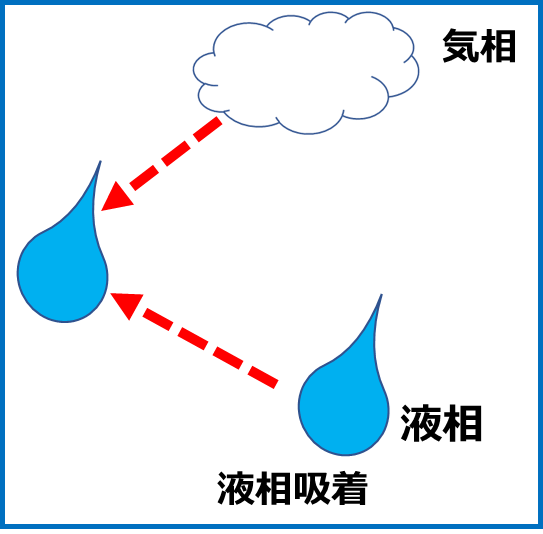
Fig4.液相吸着のイメージ
ちなみに相とは、物質の均一な部分のことをいいます。 特にその部分が気体で占められていれば気相 、液体であれば液相 、固体であれば固相といいます。
もっと科学的に解説をすると、吸着は、いずれかの相の物質の密度、またはその相の中に溶解している溶質の濃度がバルク相と界面で異なる場合で起こり、界面に比べてバルク相のほうが吸着量は多い(濃度が高い吸着を正吸着、反対に界面に比べてバルク相のほうが吸着量は少ない吸着を負吸着といいます3)(Fig5)。
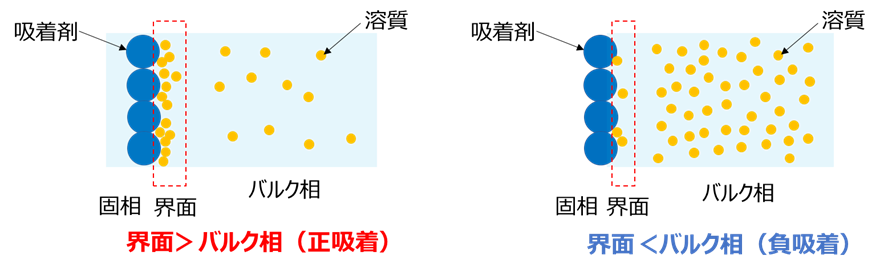
Fig5.固相吸着における正吸着と負吸着のイメージ
バルク(Bulk)とは、ある物体、流体のうち界面に触れていない部分を指し、バルク相とはそのバルク部分の均一な部分を表します4)。
界面は固相とバルク相の境界面のことです。
吸収との違い
英語ではabsorptionといい、外部のものを内に吸い込む、すっかり吸い取る、または取り入れて自分のものとすることです。科学における吸収とは、物質がある相から別の相に移動する現象、または人為的にそれを利用する方法を指します。
例えば、溶媒へのガスの吸収 溶解やゴムへの油の吸収膨潤などのように、2つの相の物質またはその中の溶質が界面を透過して相手の相の中に溶け込んでゆく現象を吸収といいます5)。
収着って?
固体が気体や溶液と接触しているとき、吸着質が固体表面に吸着して、さらには固体の内部に求核物が拡散吸収される現象をいい、化合物が形成される場合もあります。
収着は、高分子材料に対する水や有機分子の吸着において,吸着と吸収がともなって起こるときにしばしば認められます6)。
吸着等温線
吸着等温線とは、一定温度における平衡吸着量と圧力(または濃度)の関係を表したもので、一定の温度で圧力を変化させた場合の吸着量を測定して、その結果を、横軸に相対圧、縦軸に吸着した量をとってプロットしたものです。
一般に、平衡吸着量は吸着質の圧力(濃度)が高くなるほど増加しますが、その増加傾向は吸着材・吸着質の種類によって様々です。
吸着等温線は、Fig6で示すようにIUPAC(国際純正・応用化学連合)では、6種類に分類されています。
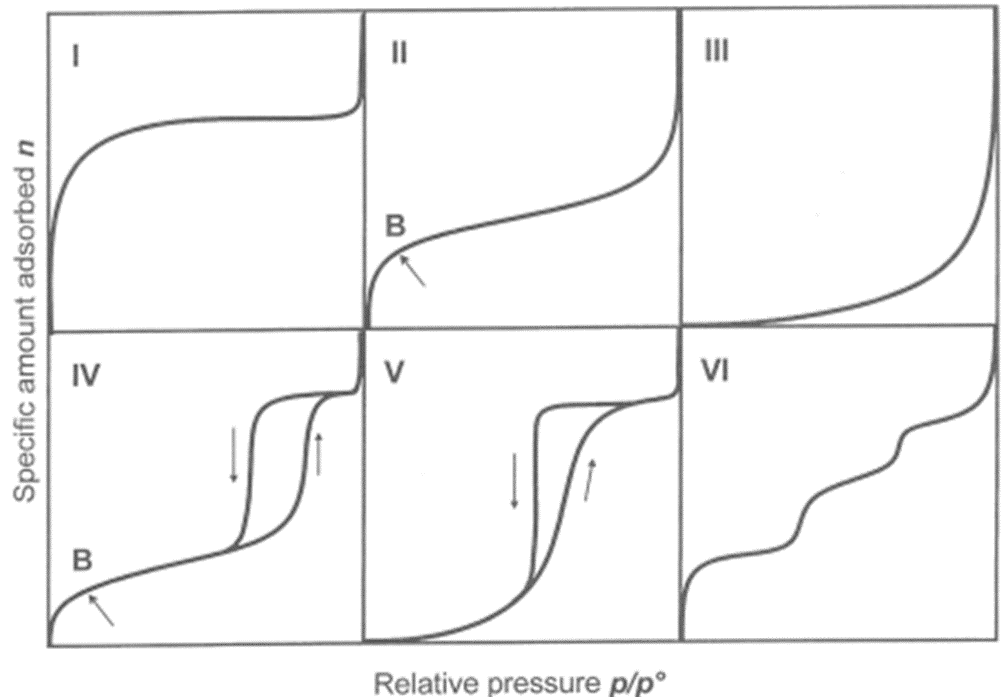
Fig6.IUPACで分類されている6種類の吸着等温線7)
Ⅰ型
圧力が増加すると吸着量は一定値に収束する傾向を示し、一般に圧力が低い場合に見られます。
Langmuirが提唱した単分子吸着理論で得られる吸着等温式と一致するため、Langmuir型とも呼ばれます。マイクロ孔やウルトラマイクロ孔を持つ吸着剤への吸着もこの型に分類され、マイクロ孔を持つサンプル、例えばゼオライトや活性炭がこの型を取ります。
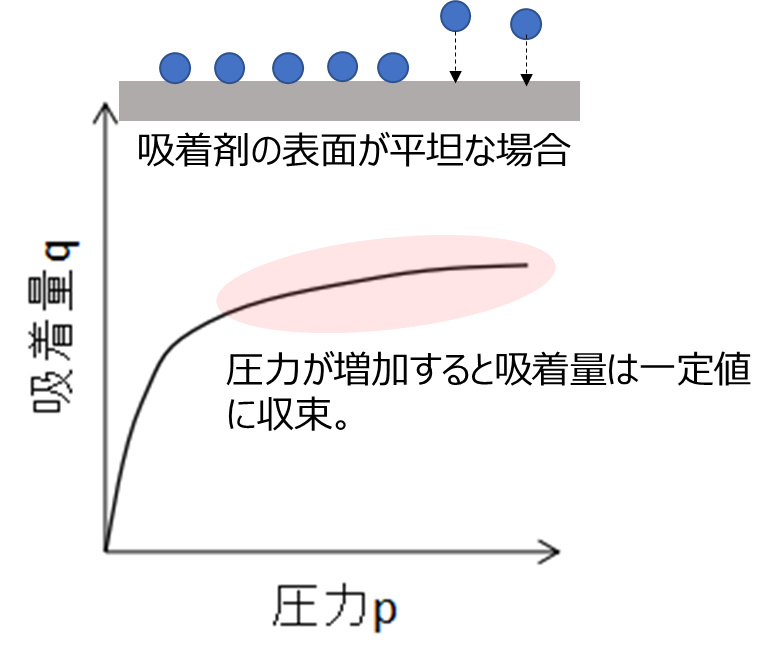
Fig7.Ⅰ型の吸着イメージと吸着等温線
Ⅱ型
多分子層吸着が行われるものはこの吸着等温線を示します。最初の飽和傾向は単分子吸着が飽和に近づくため発生しますが、さらなる圧力上昇により多分子吸着が発生することで吸着量が増加する傾向を示すのが特徴です。このような多分子吸着の理論はBrunauer、Emmett、Tellerらが提唱しており、頭文字を取りBET型とも呼ばれている。
無孔性材料。無孔性アルミナやシリカがこの型を取ります。

Fig8.Ⅱ型の吸着イメージと吸着等温線
Ⅲ型
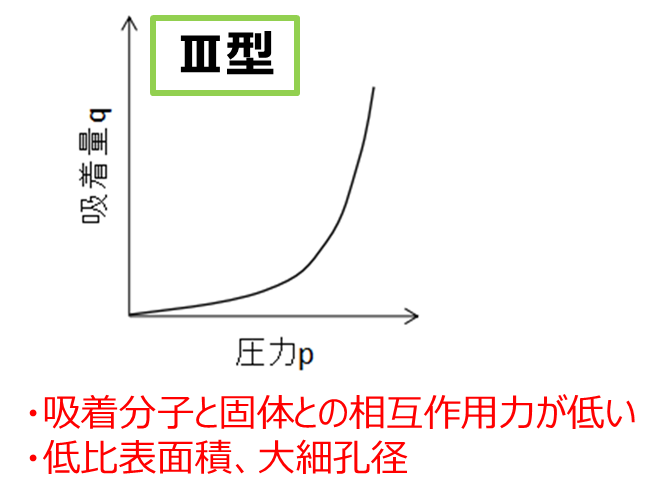
圧力が高くなるにつれて吸着量がどんどん増加する傾向を表す吸着等温線です。
水溶液から固体への吸着など、吸着剤表面と吸着質の相互作用が弱い場合に見られ、Freundlichの吸着等温式で表わすことができます。
Freundlichの吸着等温式とは、吸着剤重量あたりの平衡吸着量をv、吸着物質の流体相における濃度もしくは分圧をpとすると、温度一定の条件で、次の関係で表されます。
v=ap1/n
一般に、吸着分子と固体との相互作用力が低いものがこの型を取り、グラファイトへの水の吸着はこの型を取ります。
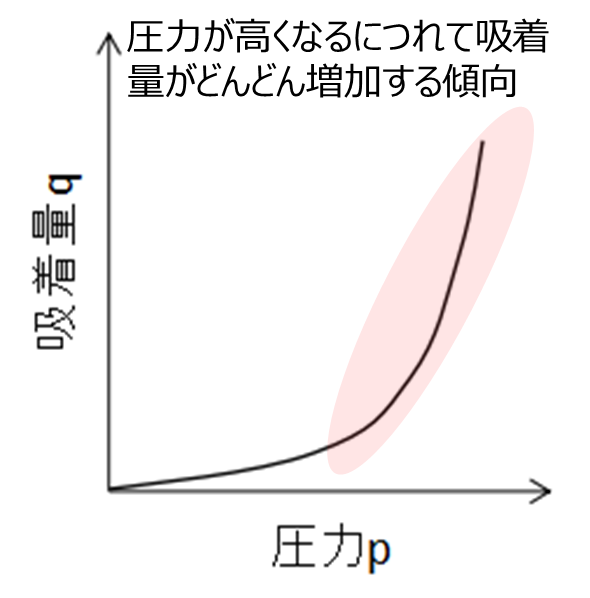
Fig9.Ⅲ型の吸着等温線
Ⅳ型
Ⅳ型はヒステリシスループを有しているのが特徴です。ヒステリシスとは吸着時と脱着時の等温線が一致し現象をいい、別名履歴現象ともいいます。
ヒステリシスが起こる理由として、2~50nm程度のメソ孔を持ち、穴の入口と孔の中で凝縮時の圧力が異なることから発生する毛管凝縮が原因です。一般的にはアルミナ粒子などがこの形式を取ります。
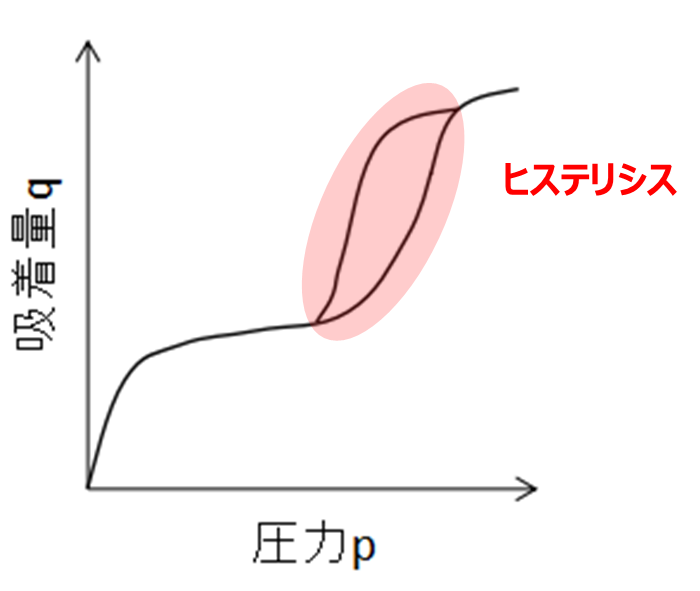
Fig10.Ⅳ型の吸着等温線
Ⅴ型
Freundlichの吸着等温式の傾向を持ちつつ、メソ孔由来のヒステリシスを持つため、Ⅲ型とⅣ型の特徴を併せ持つ吸着等温線となります。細孔を持つサンプルで吸着分子と個体の相互作用力が低もので、活性炭への水の吸着はこの型を取ります。
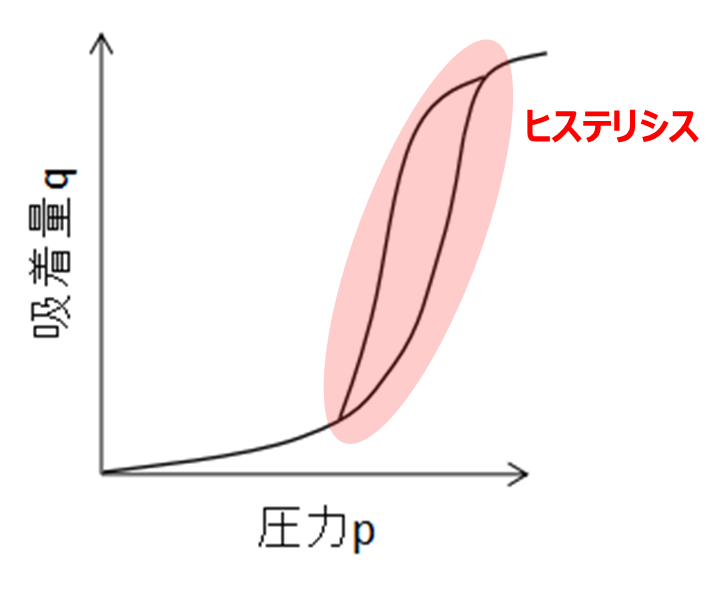
Fig11.Ⅴ型の吸着等温線
Ⅵ型
第一層の吸着が完了した後に第二層の吸着が生じるため、階段状の吸着等温線となります。
この現象は、細孔を持たず表面が均一な吸着質への多分子層吸着で見られます。
表面エネルギーが均一サンプルにこのような吸着傾向が見られ、メソポーラスシリカ、グラファイトや塩化ナトリウムのKr吸着はこの型を取ります。
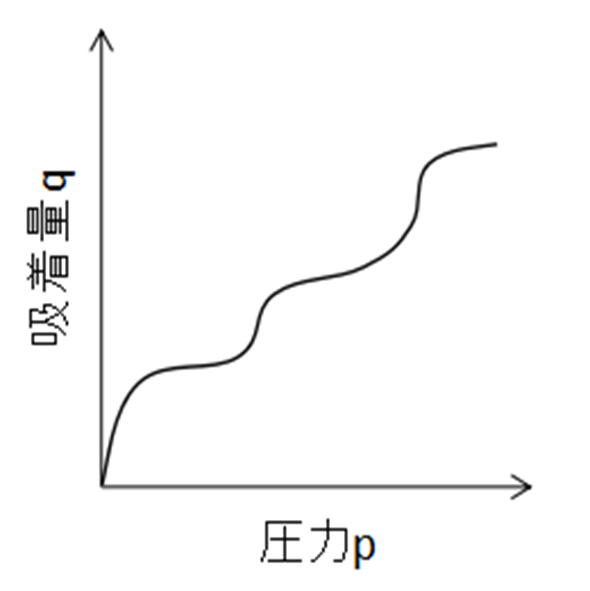
Fig12.Ⅵ型の吸着等温線
シリカゲルの吸着等温線
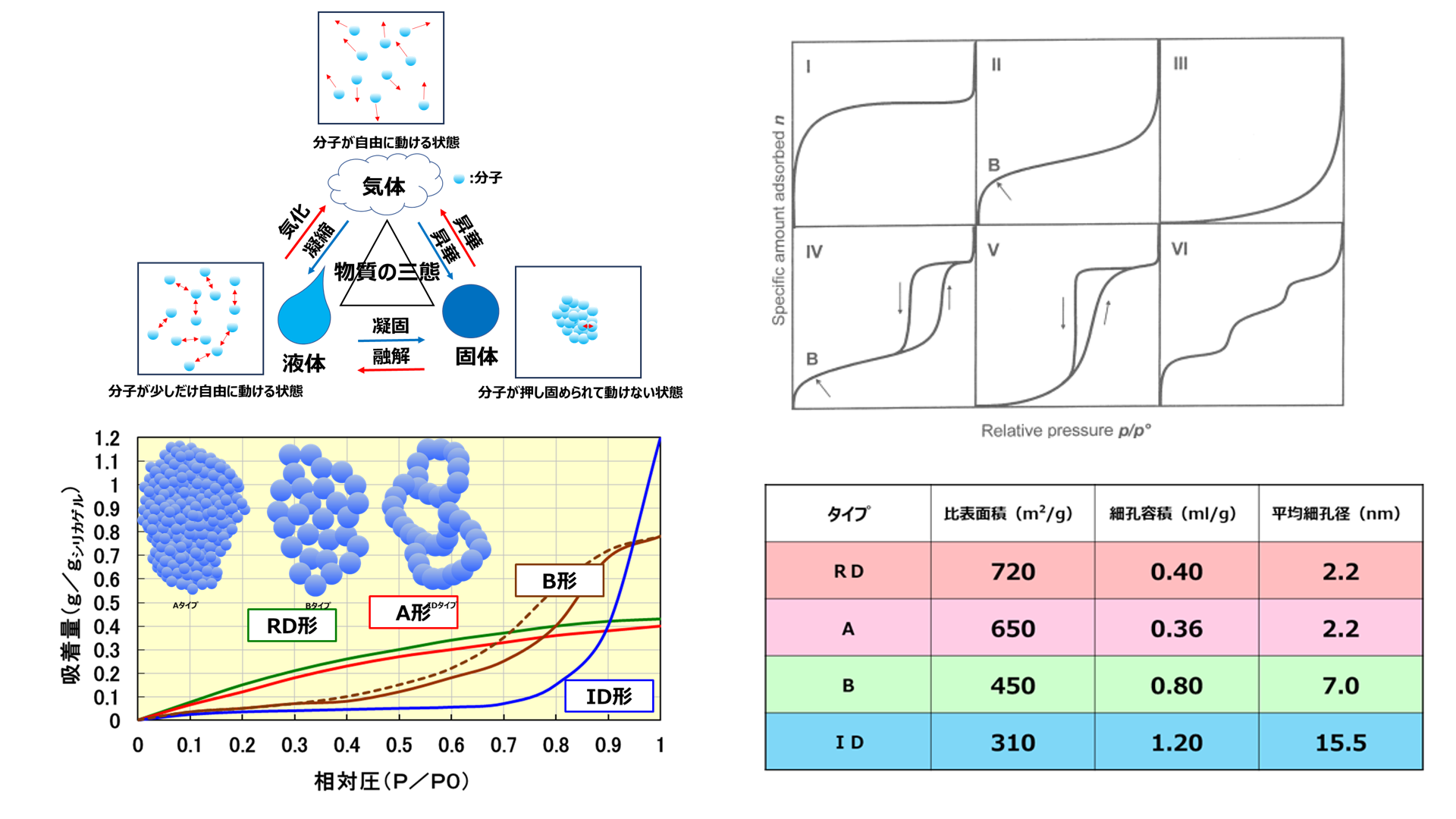
シリカゲルは、乾燥剤、調湿剤としてさまざまな分野に用いられています。このため、一般的にシリカゲルの吸着能力は常温(25℃)における水に対する吸着等温線で評価します。
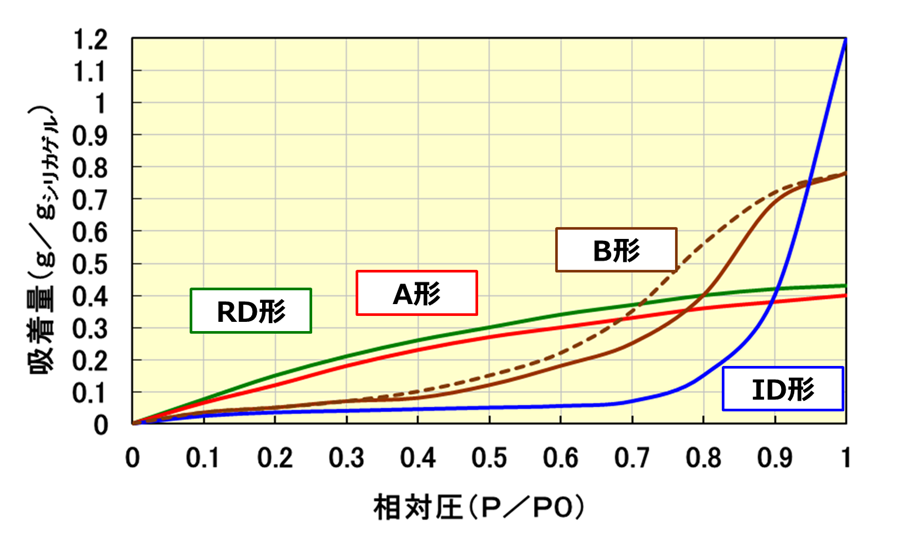
Fig13. シリカゲルの水に対する吸着等温線(25℃)8)
吸着等温線から読み取れるシリカゲルの構造と特徴
Table1にシリカゲルの比表面積、細孔容積、平均細孔径の代表値を示します。
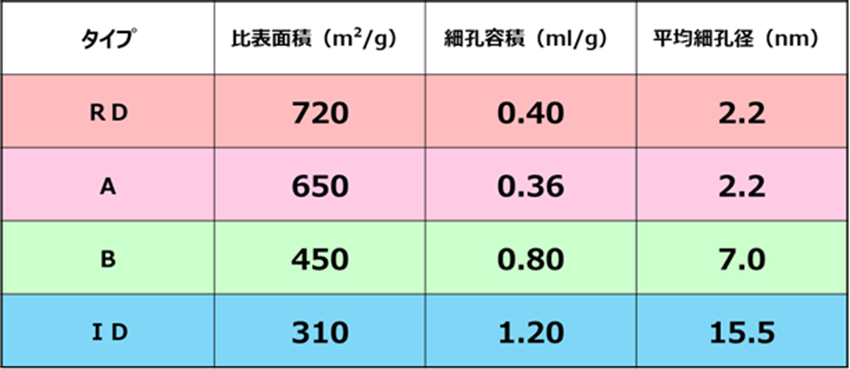
Table1.シリカゲルの比表面積、細孔容積、平均細孔径の代表値
RD形、A形シリカゲル
一般にRD、A形シリカゲルは低圧領域での吸着性能が高いため乾燥用として用いられます。
例えば、煎餅のように湿気により風味が損なわれてしまうお菓子の乾燥剤に用いられます。
吸着等温線はⅠ型を示し、このときシリカゲルの相対圧が1の場合にはRDタイプが0.42、Aタイプが0.4となり、細孔容積と一致します。
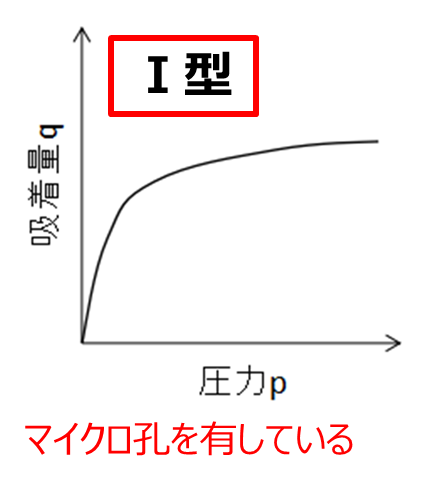
Ⅰ型の吸着等温線を示す物質は、直径2nm以下のマイクロ孔を有しているのが特徴となります。RD形、A形シリカゲルはともに平均細孔径は2.2nmを示すことからマイクロ孔を有していいます。
Fig14にRD形とA形シリカゲルの構造イメージを示します。

Fig14.RD形、A形シリカゲルの構造(イメージ)
A形シリカゲルの一次粒子の大きさは計算から4nmとなり、このように小さな一次粒子が集まって細孔が形成されています。同様にRD形シリカゲルは3.8nm程度の一次粒子が集まって細孔が形成されていて、若干ではありますが、形成される細孔の直径は小さくなりますので、低圧領域での吸着性能が高いことからより水を吸着する力が強いことになります。
また、RDシリカゲルの一次粒子の大きさはA形シリカゲルに比べ若干小さい反面、凝集の状態がA形シリカゲルに比べ若干租いため、RD形シリカゲルの細孔容積は若干大きくなります。
B形シリカゲル
B形シリカゲルは、相対圧0.5付近から吸着量が上昇して、最終的に相対圧が1となった時に、0.8となり細孔容積と一致します。また、ヒステリシスを有しているためⅣ型の吸着等温線を取ります。
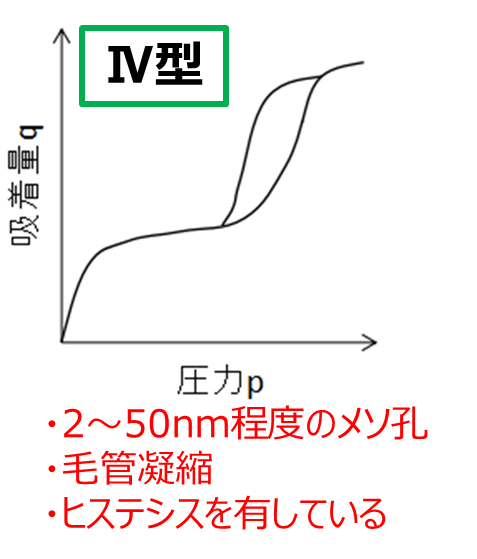
Ⅳ型の吸着等温線を示す物質は、直径2nm~50nmのメソ孔を有しているのが特徴となります。
B形シリカゲルはともに平均細孔径は7.0nmを示すことからメソ孔を有していいます。
Fig15にB形とシリカゲルの構造イメージを示します。
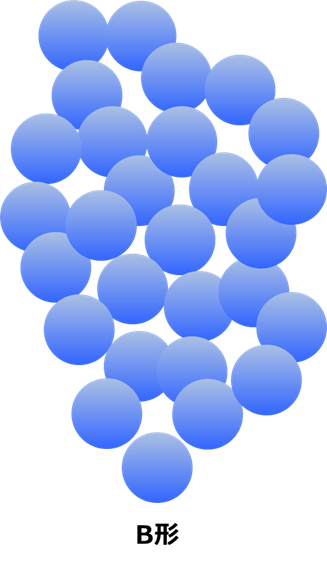
Fig15.B形シリカゲルの構造(イメージ)
B形シリカゲルは計算上6nm程度の小さな一次粒子が集まって7nm程度の細孔が形成されていす。また、毛管凝縮による吸着が行われるため、吸脱着によるヒステリシスを有しています。
毛管凝縮ついては、シリカゲルの物理吸着のところで詳しく述べます。
ID形シリカゲル
ID形シリカゲルの吸着等温線は、相対圧0.7から急激に吸着量が増加して、最終的に相対圧が1となった時に、1.2となり細孔容積と一致しています。
Ⅲ形の吸着等温線は、吸着分子と固体との相互作用の力が低いため、低比表面積かつ細孔径が大きなものがこの形を示します。
このため、ID形シリカゲルの吸着等温線はⅢ型をとります。
ID形シリカゲルの構造をFig16に示します。

Fig16.ID形シリカゲルの構造(イメージ)
ID形シリカゲルは、他のシリカゲルに比べ、一次粒子径が大きく、かつ重合(エージング)も進んでいるため、比表面積が低く、細孔容積も大きなものとなります。
このように吸着等温線からもシリカの物性情報を得ることができます。
化学吸着と物理吸着
吸着は、その性質から化学吸着、物理吸着に大別されます。
化学吸着
化学吸着とは固体表面に原子や分子が吸着する現象のなかで、吸着の原因が化学結合生成や電荷移動相互作用によるものである吸着のことと定義されています。 金属や金属酸化物などに化学吸着される気体分子や気体原子は多く、次のような特徴があります。9)
・物質による特異性が強い
・吸着速度が遅い
・吸着熱が大きく、数百 kJ mol-1である
・温度依存性が大きい
・単分子層吸着のみが起こる
・可逆的な吸着
通常、気体分子や蒸気からの吸着は発熱を伴うが、化学吸着の吸着熱は非常に大きく80~400 kJ mol-1です。また、化学吸着の速度は遅く、温度依存性が大きい。結合生成の活性化エネルギーをEとしたとき化学吸着はexp−ERに比例します。
また、化学吸着は非可逆的である。固体表面原子と吸着気体分子との化学結合生成が吸着の駆動力であるため、単分子吸着のみが起こることになります。
シリカゲルの化学吸着
Fig17に示すようにシリカゲルには、孤立シラノール、内部シラノール基、水素結合性シラノールの3種類のシラノール基が存在します。水(吸着水)はシリカゲルの孤立シラノール基(Si-OH)と水との水素結合により吸着して、この吸着は化学吸着の一種です。
また、水素結合性シラノール基は、シラノール基どうしが互いに水素結合(化学結合)で引き合っています。
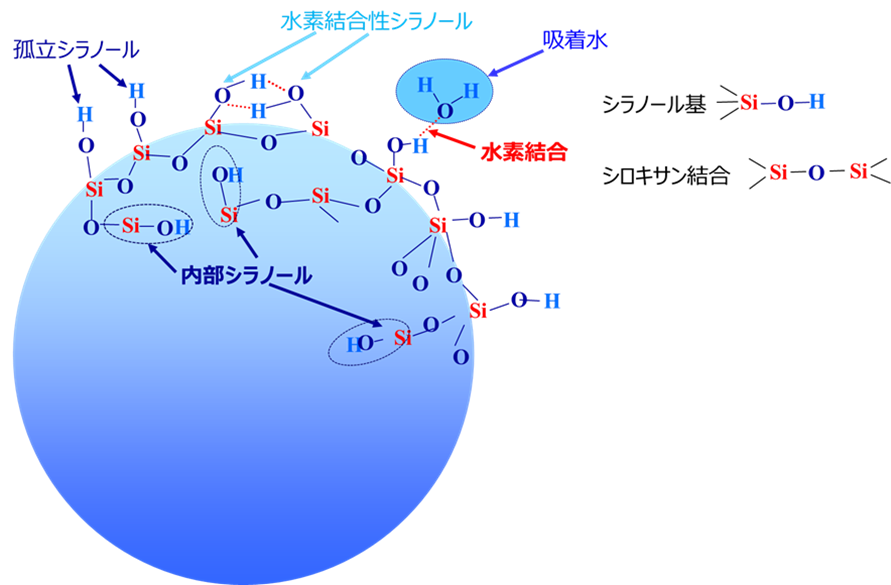
Fig8. シリカゲル表面の状態(イメージ)10)
物理吸着
物理吸着とは固体表面に原子や分子が吸着する現象のなかで、吸着の原因が主に気体分子と表面原子のファンデルワールス力 (van der waals相互作用) による吸着で、次のような特徴があります。9)
・物質による特異性が少ない
・吸着速度が早い
・吸着熱が小さく、~20 kJ mol-1である
・温度依存性が小さい
・多分子層吸着が起こる
・可逆的に脱離し、解離はしない
通常、気体分子や蒸気からの吸着は発熱を伴い、この吸着熱は物理吸着では気体の凝縮熱よりやや大きい程度の~20 kJ mol-1です。
シリカゲルの物理吸着
シリカゲル表面にシラノール基に吸着された吸着水は、内部シラノール基にも同様に吸着されます。内部シラノール基の表面に吸着された吸着水は水膜となり層を形成します。この層を他分子吸着層といいます。このときシリカゲルの細孔の内壁は毛細管現象により周囲の水を引っ張ることで表面張力が増加します。表面張力の増加に伴い、水の分子運動は低下して、気体側から液体側にずれることで凝縮されます。
毛細管現象とは、photo1 で示すように細管の径を細くすればするほど液面が高くなる物理現象で、管径が細いほど管の壁面と液体の引き合う力がより強くなる現象です11)。

Photo1. 毛細管現象
Fig9にシリカゲルの物理吸着のイメージ図を示します。
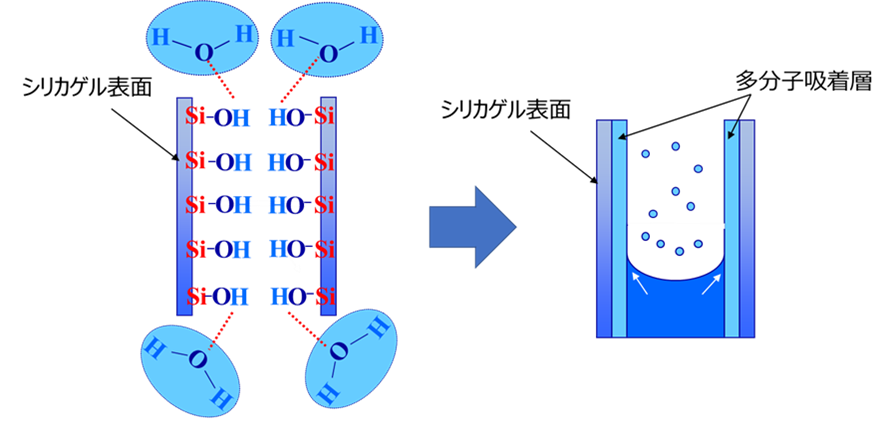
Fig9. シリカゲルの物理吸着(イメージ)
シリカゲルは、化学吸着、物理吸着の二段階で行われますので、高い吸着性能を有しています。この吸着は、比表面積、細孔容積、細孔径を制御することでRD、A、B、IDタイプで異なった吸着を示します。
また、フュームドシリカ、沈降性シリカなど凝集により形成されたマイクロ孔、メソ孔を有しているシリカも、シリカゲルと同様に化学吸着、物理吸着能を有しています。しかし、シリカゲルほど堅牢な細孔構造を有していないため、一般的に細孔は崩れやすくの強度は弱いものとなります。
まとめ
シリカは、表面や細孔を利用して物質を吸着します。この吸着機能を利用して水をはじめとして、有害ガスや重金属などの有害物を吸着、最近では二酸化炭素の吸着担体としても注目されています。
なかでもシリカゲルは一次粒子径の凝集により堅牢な細孔と比表面積を有していて、一次粒子の大きさと密度をコントロールすることで、RD形、A形、B形、IDに作り分けることができます。
このためそれぞれの吸着の状態が異なり、RD、A形はⅠ型の吸着等温線、B形はⅣ型の吸着等温線、ID形はⅢ型の吸着等温線をそれぞれ取ります。
また、シリカゲルは、化学吸着と物理吸着の2段階で水を吸着して、特にRD形、A形は水吸着する力が強いため乾燥用途、B形シリカゲルはヒステリシスを有するために調湿用途、ID形は水を吸着する力は非常に弱い反面、細孔容積が大きいため水をたくさん保持できるという特徴があります。
また、フュームドシリカ、沈降性シリカなど凝集により形成されたマイクロ孔、メソ孔を有しているシリカも、シリカゲルと同様に化学吸着、物理吸着能を有しています。しかし、シリカゲルほど堅牢な細孔構造を有していないため、一般的に細孔は崩れやすくの強度は弱いものとなります。
参考文献
1) Tri it 5分でわかる! 物質の3態 https://www.try-it.jp/chapters-8873/sections-8913/lessons-8922/を参考に筆者作成
2) Lab Brands https://lab-brains.as-1.co.jp/enjoy-learn/2023/02/41766/
3) 近藤ら 吸着の科学(第3版)丸善出版 p.4(2019)
4) DAIKIN 分子ソフト&インフォマティクス 用語解説 https://www.comtec.daikin.co.jp/SC/glossary/bulk.html
5) 近藤ら 吸着の科学(第3版)丸善出版 p.5(2019)
6) 粉体工学用語辞典 http://www.sptj.jp/powderpedia/words/10945/
7) L. Chmielarz, P. Kuśtrowski, A. Rafalska-Łasocha, R. Dziembaj, Appl. Catal.B., 58 pp. 235-244 (2005)
8) 富士シリシア化学(株)フジシリカゲルカタログをもとに筆者作成
9) 化学徒の備忘録(かがろく) 物理吸着と化学吸着の特徴について https://onl.sc/RvyC8xm
10) 近藤ら 吸着の化学 丸善 pp. 204-208 (1991)をもとに筆者作成
11) 岡田ら 粉体層の構造因子と毛管力 日本鉱業会誌/98 1137 (1982)


-300x188.png)

-300x188.png)
-300x188.png)
コメント
コメント一覧 (1件)
[…] 吸着の詳細については記事『シリカと吸着』を参照ください。 […]