シラノール基とは化学式ではSi-OHと表され、シリカを理解する上で非常に重要な結合になります。
更に、シリカやシロキサン結合と密接な関係があります。また、シラノール基は、シリカ単体の性質にとどまらず、材料全体の性能を作用する重要な因子でもあります。
シラノール基は、シリカ、シロキサン結合と密接な関係があるので、シラノール基を説明する前に、まずはシリカ、シロキサン結合について簡単に解説します。
シリカ(SiO2)
シリカ(英:silica)の組成式は、SiO2で表すことができ、二酸化ケイ素(SiO2)、もしくは二酸化ケイ素によって構成される物質の総称です。シリカという呼び名のほかに無水ケイ酸、ケイ酸、酸化シリコンと呼ばれることもあります。
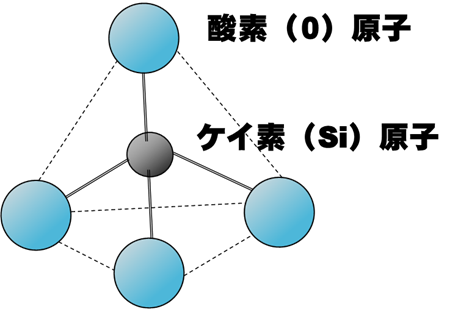
Fig1. SiO4の四面体構造1)
実際シリカは手が4本のため、SiO2としてはおらずSiO4の四面体構造で存在しています。
しかし、Siの周りの4つの酸素は不安定で常に何かと結びつきたがります。
合成シリカの原料となるケイ砂や石英をはじめとするケイ酸塩鉱物は、SiO4四面体がO原子と隣り合うSi原子に共有されて結合しています。
この共有している酸素を共有酸素原子といいます。
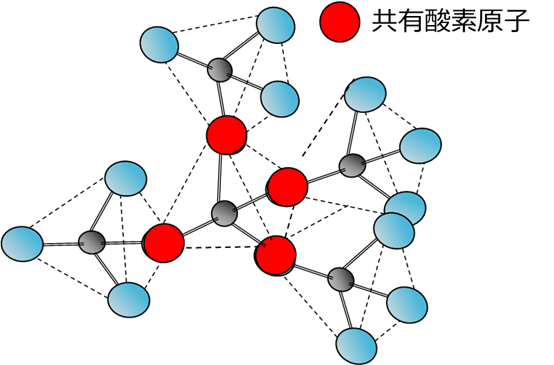
Si:1個
O:4×1/2=2個
Fig2. SiO4の四面体構造の共有と共有酸素原子
このため、SiO4四面体はO原子が隣り合う2個のSi原子に共有されて結合しているため、一般的に組成を示すときはSiO2として表現されます。
シロキサン結合
シロキサンとは、ケイ素(Si)と酸素(O)が交互に結合して、Si-O-Siポリマーが形成された状態のことをいいいます。シロキサン結合と呼ばれるシリコーンの主骨格となっています。
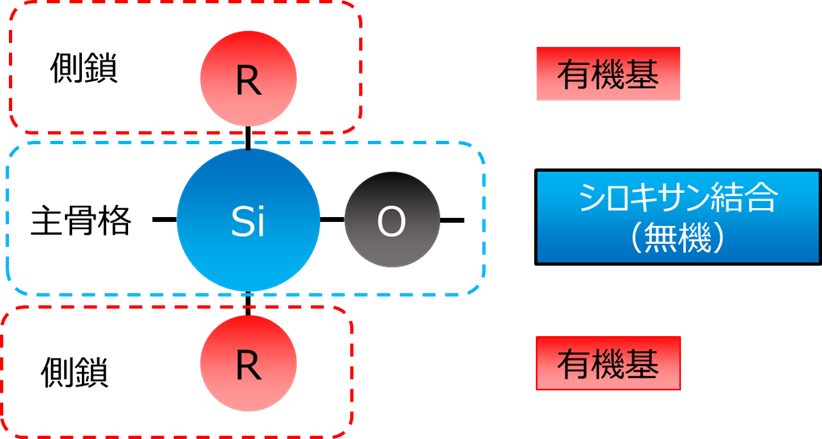
Fig3. シリコーンの構造とシロキサン結合
シラノール基
シラノール基(Si-OH)は、シリカ表面に存在するもので、孤立(isolated)、ビシナル(vicinal:隣り合うシラノール基が水素結合している)、ジェミナル(geminal)の3つのタイプが知られています(Fig3)。個々の状態などによって程度の差はありますが一般に弱酸性を示します。
基とは官能基や炭化水素基などひとまとまりの原子団を指します。
官能基は、有機化合物を特性づける原子団で、機能原子団あるいは作用基ともいい、同じ官能基をもつ有機化合物は性質や反応性が類似しているので、有機化合物は官能基によって分類されます。
シリカの成分(Si)も炭素(C)と族が同じため官能基によって分類されます。
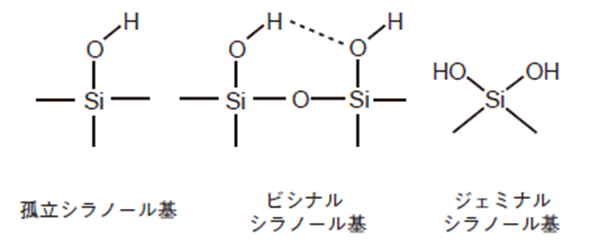
Fig4. シラノール基とその種類2)
シラノール基の酸性度
上述したようにシリカ中のシラノール基は水中では弱酸性を示します。しかし、塩化マグネシウムや塩化カルシウム等の2価の金属塩を添加すると、イオン交換によりプロトン(H+)が生じます。プロトンは酸のもとであり、このプロトン(H+)が多いほど酸性度が高くpH(ピーエッチ、ペーハー)が低くなります。
この状態を化学式で表すと次のようになります。
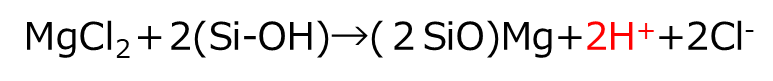
シリカを水の中で攪拌させてスラリー状にしたものに塩化マグネシウム等の2価の金属塩を加えることにより、シラノール基からプロトンが外れます。反応は水中で起こっているために、プロトンは塩化物イオンと水中に残ったままとなり、塩酸が電離している状態となります(Fig5)。
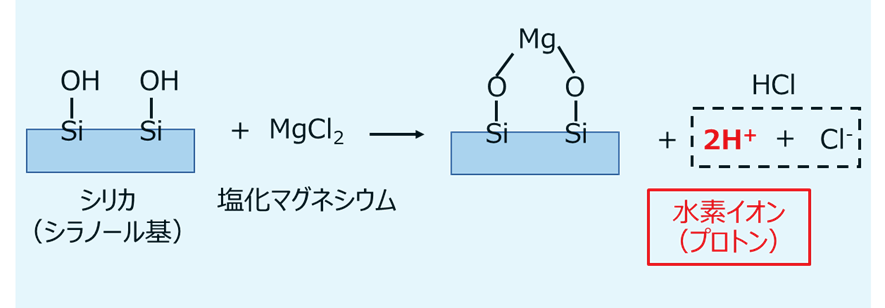
Fig5. 塩化マグネシウム添加によるシラノール基からのプロトン発生のイメージ
Dr. Aristovらは、シリカゲルのシラノール基とLiBr、Na2SO4、CaCl2、MgSO4、CuSO4塩の関係について検討を行い、シリカゲル表面への吸着にプロトンの増加は以下のような傾向があることを見出しています。3)
LiBr < Na2SO4 < CaCl2≈ MgSO4 < CuSO4
更に、シリカゲルの表面シラノール基からのシリカ表面のプロトン電荷は、1-3mol/Lの塩溶液中では、水と比較して3-10倍に増加することも見出しています。3)
このように水中でシラノール基は、金属塩の水溶液によりプロトンを生じるため水溶液のpHが急激に低くなるため、pHの調整が困難になったり、装置内部の腐食を促進してしまう場合があるため注意が必要です。
pHとは
pHは次の式で表されます。

純粋な水は水分子のまま安定しているわけではなく、水素イオンと水酸化イオンに電離をしたり、水分子に戻ったりを繰り返してします。この水素イオンと水酸化物イオンとして存在する割合を繰り返しています。
この電離している割合を電離度(α)といいます。

このとき生じているH+の濃度が高いか低いかを示す尺度がpHです。水中のpHは溶けている物質や温度に応じて様々な値をとります。
更に、H+とOH–は、両者の濃度を掛けた値が一定となります。

(1)の式を用いて換算すると(3)になります。

普通は両者を足して14が最大となります。
このとき液性とpHは次のような関係があります。
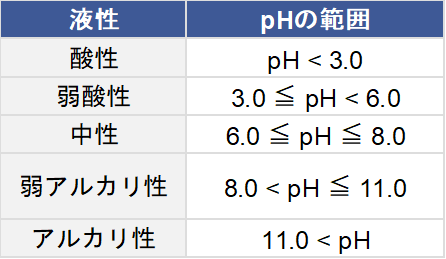
Table1. 液性とpHの関係4)
湿度インジケーターシリカゲルへの展開
筆者は宮崎大学と共同で、シリカ中のシラノール基に金属塩を作用させることで生じるpHの変化を用いて湿度インジケーターシリカゲルの開発に成功しています。
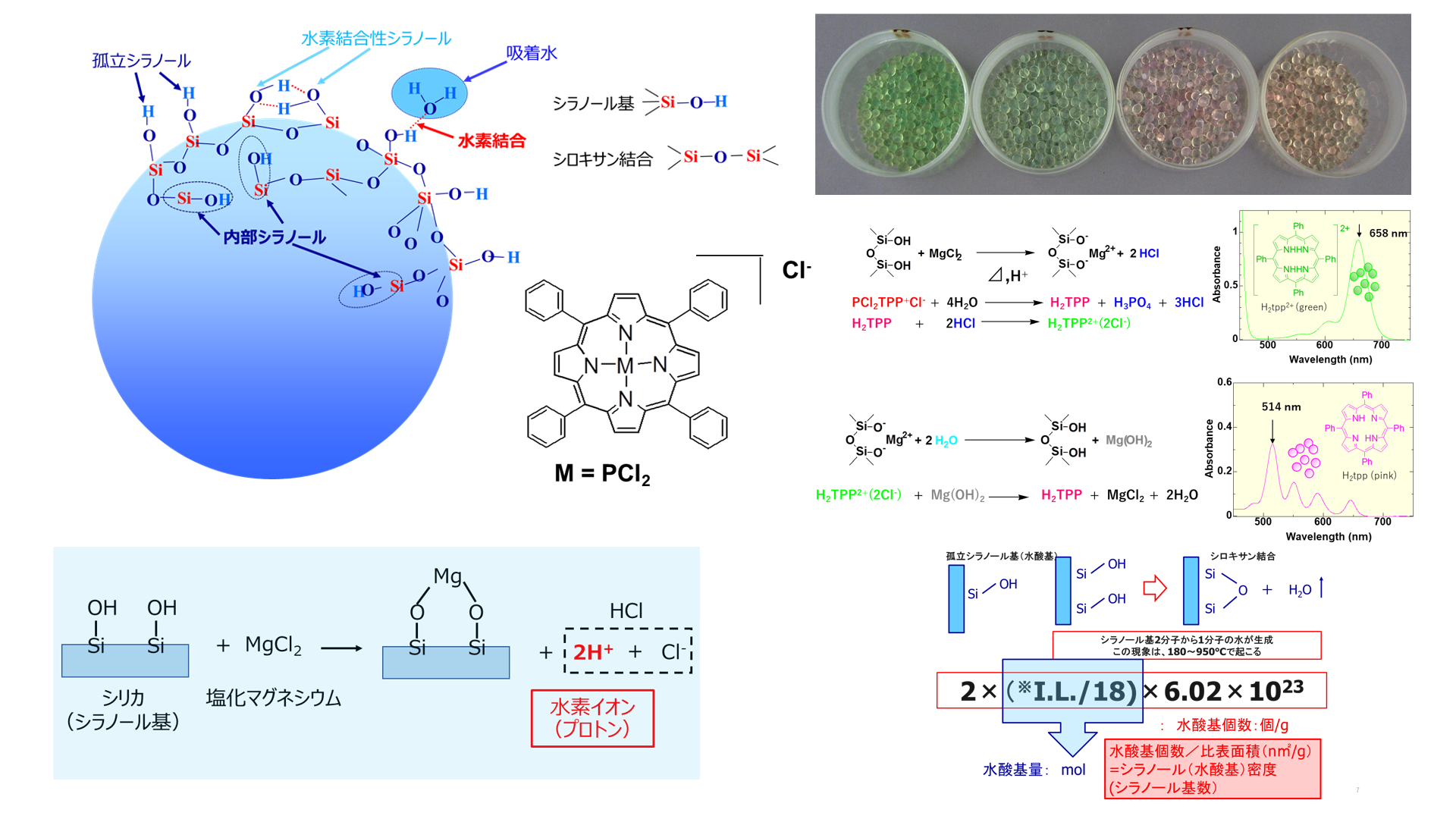
この湿度インジケーターシリカゲルには、湿度インジケーター剤として安全性の高いテトラフェニルリンポルフィリン塩化物塩(PCl2TPP+Cl–)が用いられていて、乾燥時には緑色に発色し、相対湿度が20%では黄緑色、中湿度領域のRH50%ではピンク色、高湿度領域のRH90%では橙色を示し、従来の湿度インジケーターシリカゲルより視認性が高いことが特徴です。
http://www.fujigh.co.jp/fuji_si_gel.htm
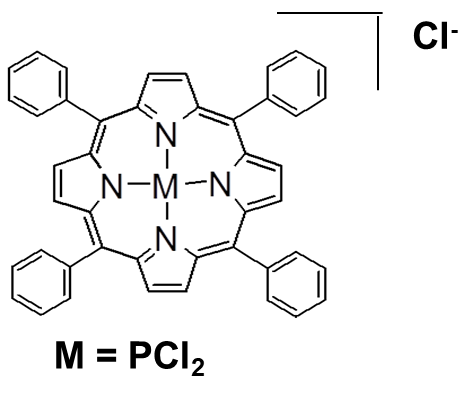
Fig6. テトラフェニルリンポルフィリン2塩化物塩の構造5)

Fig7. 湿度インジケーターシリカゲルの変色範囲6)
湿度インジケーターシリカゲルの発色機構
乾燥時
この湿度インジケーターシリカゲルの発色機構とシラノール基には密接な関係があり、塩化マグネシウムなどの2価の金属塩をシリカゲル表面のシラノール基に作用させることでプロトンを発生させて、このプロトンをテトラフェニルポルフィリン(H2TPP)が受け取るとこで緑色に発色します。
このときプロトン化したテトラフェニルポルフィリン(H2TPP2+)は658nmの可視光領域に吸収を持つため、緑色に発色します。
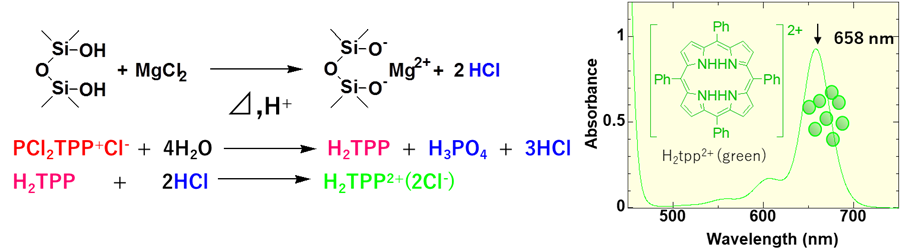
Fig8. 湿度インジケーターの乾燥状態のメカニズム7)
吸湿時
吸湿により、O-Mg-O(O– Mg2+ O–)の部分がシラノール基に戻り、Mgは水酸化マグネシウム(Mg(OH)2)が生成します。H2TPP2+は、生成したMg(OH)2と反応してH2TPPとなり、H2TPPがRH50%の時514nmの可視光領域に吸収を持つため、ピンク色に発色すると考えられています。
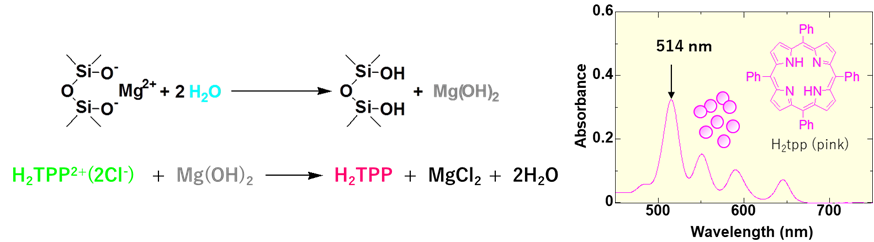
Fig9. 湿度インジケーターの吸湿状態のメカニズム7)
また、このポルフィリンの発色機構を用いて、塩化マグネシウムを用いてシラノール基から生ずるプロトンの酸の強さを顕微吸光度分析法によって測定した結果、最も強いものでpH 1.2程度の強酸性有してることが報告されています8)。
さらに、この強酸性を利用して硫酸を用いずニトロ化反応ができることが報告されています。9)
シラノール基数(シラノール基密度)の定量方法
加熱水分減量法
単位表面積当たりのシラノール基数は加熱水分減量法により算出可能です
通常、シリカの表面は、シラノール基の水素結合に引き寄せられ、水分子は表面に吸着していて180℃に加熱することで孤立シラノール基が現れます。 Fig8にシリカゲルの表面状態を示します。
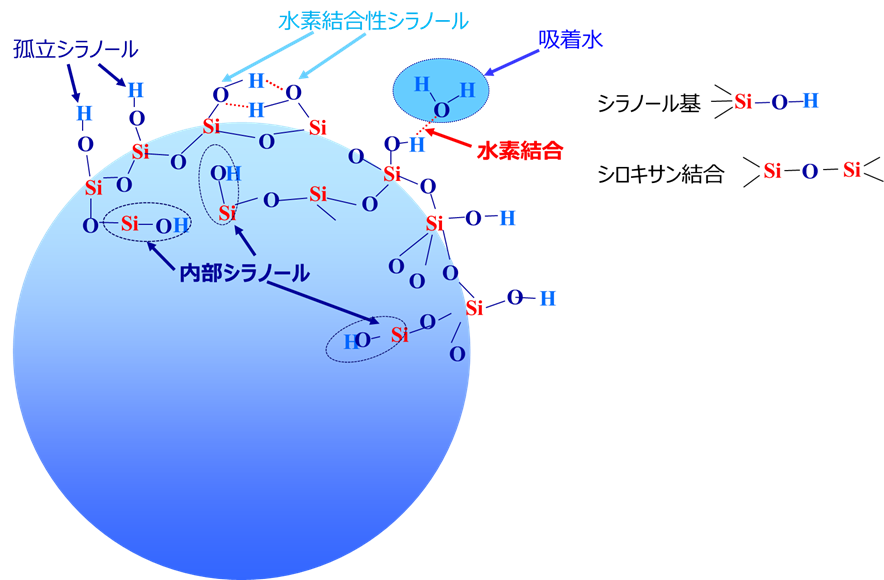
Fig8. シリカゲル表面の状態(イメージ)11)
また、シラノール基から水が取れ脱水縮合したものをシロキサンといい、Si-O-Siをシロキサン結合といいます。シラノールからシロキサンへの変化は、温度によって変化し950℃ですべてシロキサン結合になってしまいます。
シリカとシロキサンの関係からシラノール基数を求めることができます。
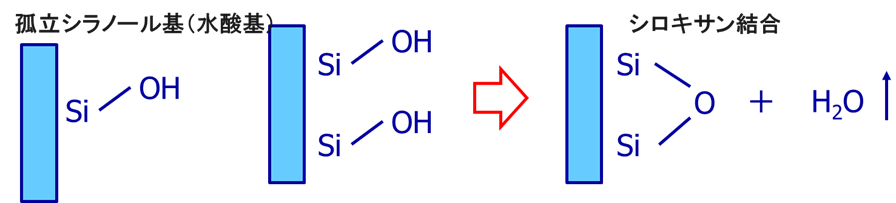
Fig5. シラノール基とシロキサンの関係
孤立シラノール基2分子から1分子の水が生成この現象は、180~950℃で起こります。
この時に外れたシリカ1g当たりの水の量は、Ignition Loss(I.L.)で表すことができます。
このI.L.を水の分子量(18)で除して2をかけて、アボガドロ定数(6.02×1023)をかけることにより、シリカ1g当たりの水酸基量(個/g)が求められますが、この状態では非常に数が多すぎて見当がつきません。このためnm2当たりの個数として算出するのが一般的です。
シリカ1g当たりのシラノール基数 = 2×(I.L./18)×6.02×1023
シリカ1nm2当たりのシラノール基数 = 2×(I.L./18)×6.02×1023 / SA×1018
SA: シリカの比表面積 (m2/g)
つまり、I.L.と比表面積がわかればシラノール基数は求めることができます。
計算例
計算例
一般的にRD形シリカゲルの比表面積は700m2/g程度、I.L.は6.5wt%程度といわれています。
また、ID形シリカゲルの比表面積は300m2/g程度、I.L.は2.5wt%程度といわれています。
この値から、RD形シリカゲル、ID形シリカゲルの1nm2あたりのシラノール基数は次のように求めることができます。
RD形シリカゲルのI.L.は6.5wt%ということからシラノールからシロキサン結合に変化するときにRD形シリカゲル1g当たり0.065gの水が取れることになります。
同様に、ID形シリカゲルでは0.025gの水が取れることになります。
このとき、シリカゲル1g当たりのシラノール基数は
RD形 2×(0.065 / 18)×6.02×1023=4.3×1021個 / SiO2 1g
ID 形 2×(0.025 / 18)×6.02×1023=1.7×1021個 / SiO2 1g
比表面積をnm2になおすと
RD形 700×1018 nm2 / SiO2 1g
ID 形 300×1018 nm2 / SiO2 1g
1nm2 あたりにすると
RD形 4.3×1021 / 7.0×1020 = 6.1個 / nm2
ID 形 1.7×1021 / 3,0×1020 = 5.7個 / nm2
IDでもRDでも単位面積あたりのシラノール基数は、ほぼ同数であることがわかります。
よって、シリカゲルのシラノール基数は5~6個 / nm2程度ということになります。
一方、フュームドシリカのシラノール基数2~3個でシリカゲルのような湿式シリカの半分といわれています。12)しかし、フュームドシリカは数珠状の一次粒子が集まった構造をしているため細孔が無く、内部シラノール基が無いため、シリカゲルに比べて個々のシラノール基の活性が高くなります。
その他の定量法
シラノールを定量する方法は、近赤外吸収分光分析法、個体Si NMR分析法、重水素置H1NMR、滴定法、TOF-SIMS法、化学修飾XPS、グリニャール試薬法、ジメチルジクロロシラン法、水酸化リチウム法、クロロシランのラベル化剤など多岐にわたる手法があります。
しかし、特別な試薬や装置を用いる必要があるため、一般には加熱水分減量法がよく用いられています。
しかし、絶対定量ができない、処理が煩雑、水分による妨害、反応性と比反応性のシラノール基が区別できないこと、感度や精度など多くの問題があります。13)
まとめ
シラノール基は化学式ではSi-OHと表されます。また、シリカ単体の性質にとどまらず、材料全体の性能を作用する重要な因子でもあります。
通常、シラノールは弱酸性ですが、水中で塩化マグネシウム等の2価の金属塩を添加することでプロト(H+)を放出します。このようなプロトン放出を利用して筆者は宮崎大学との共同研究を経て、より安全性の高い湿度インジケーターの開発に成功して商品化に結び付けることができました。
また、このときの酸の強さは非常に強く、pHが1.2程度の強酸性を示す場合もあるため、この性質を利用して硫酸を用いないニトロ化にも成功をしています。
このように筆者は長年宮崎大学と共同研究を行ってきましたが、どの研究にもシラノール基が関わっていたといっても過言ではありません。更に今後は、これまでの知見をプロトン輸送体に展開することで、プロトンポンプ機能を利用したATP合成14)や、燃料電池15)への利用ができるものと考えております。
参考文献
1)斉藤喜彦 訳 ヘスロップジョーンズ無機化学(上)第10刷 1992年 pp. 423-425
2)島津製作所https://www.an.shimadzu.co.jp/service-support/technical-support/analysis-basics/hplc/faq/principle1/lctalk-91intro/index.html
3)Larisa G. Gordeeva et.al, Impact of phase composition on water adsorptionon inorganic hybrids “salt/silica”, Journal of Colloid and Interface Science 301 p. 687 (2006)
4)鈴研株式会社 https://www.suzuken-ltd.co.jp/choose/ph/
5)特許24708973 水検出用組成物、および水検出用インジケーター p.2 (2009)
6)富士シリシア化学株式会社 インジケーターF テクニカルブレタン p. 2(2013)
7)Yoshiyuki Fueda et. al Porphyrin / MgCl2/ silica gel composite as a cobalt-free humidity indicator Chemistry Letters Vol. 36, No. 10 pp. 1246 (2007)
8)ポルフィリンをpH指示薬に用いる顕微吸光光度分析によるマグネシウム塩-シリカゲル複合固体の酸性度測定 分析化学 61(10) pp. 854-855 (2012)
9)Solid-phase aromatic nitration with Mg(NO3)2 on silica gel Green chemistry letters and Reviews (2016)
10)JIS K 1150 (1994) シリカゲル試験方法 pp. 8-9
11)近藤ら 吸着の化学 丸善 pp. 204-208 (1991)をもとに筆者作成
12)落合 満 フュームドシリカ エアロゾル研究 Vol.5 No.1 p33 (1990)
13)島岡 千喜ら シリカ表面のシラノール基の定量 The TRC News p. 1 (2019)
14)福岡大学 http://www.sc.fukuoka-u.ac.jp/~bc1/Biochem/photosyn.htm
15)Steven J. Hamroc et. al Proton Exchange Membranes for Fuel Cell Applications Journal of Macromolecular Science, Part C Polymer Reviews Volume 46 Issue 3 (2006)


-300x188.png)

-300x188.png)
-300x188.png)
コメント
コメント一覧 (2件)
[…] また、合成シリカにはシラノール基があり、乾燥減量の105℃ではシリカの吸着水のみが除去され、シラノール基の脱水縮合が起こりません。このため、シラノール基の水分を除去するため850℃の強熱減量で加熱を行います。このため、強熱減量では、吸着水とシラノール基の水分の両方の含水量が測定されることになります。詳細につきましては、記事『シラノール基』を参照ください。 […]
[…] シラノール基についての詳細は、記事シラノール基を参照ください。 […]